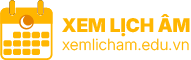Năng lượng hoạt hóa là khái niệm quan trọng trong hóa học và vật lý, giúp giải thích cách các phản ứng hóa học xảy ra và lý do tại sao một số phản ứng nhanh, trong khi một số khác lại chậm. Với vai trò thiết yếu trong nghiên cứu và ứng dụng thực tế, năng lượng hoạt hóa đã trở thành nền tảng cho nhiều ngành công nghiệp và khoa học hiện đại.
1. Năng lượng hoạt hóa là gì?
Năng lượng hoạt hóa (Activation Energy – Ea) là mức năng lượng tối thiểu mà các phân tử phản ứng cần đạt được để xảy ra phản ứng hóa học. Đây là rào cản năng lượng ngăn cản các chất phản ứng ngay lập tức chuyển đổi thành sản phẩm.
Năng lượng hoạt hóa được biểu diễn bằng đồ thị năng lượng, trong đó:
- Chất phản ứng: Ban đầu có mức năng lượng thấp.
- Năng lượng hoạt hóa: Đỉnh năng lượng cần vượt qua để đạt trạng thái chuyển tiếp.
- Sản phẩm: Có mức năng lượng thấp hơn (trong phản ứng tỏa nhiệt) hoặc cao hơn (trong phản ứng thu nhiệt) chất phản ứng.
Ví dụ cụ thể:
- Đốt than đá: Than cần được đốt cháy ở nhiệt độ cao (kích hoạt bằng nhiệt độ từ ngọn lửa) để phản ứng oxy hóa xảy ra. Nhiệt từ ngọn lửa là năng lượng hoạt hóa.
- Phản ứng hóa sinh: Trong cơ thể, enzyme đóng vai trò giảm năng lượng hoạt hóa, giúp phản ứng xảy ra dễ dàng mà không cần nhiệt độ cao.
Năng lượng hoạt hóa có sự tham gia xúc tác của enzyme
2. Vai trò của năng lượng hoạt hóa
Năng lượng hoạt hóa ảnh hưởng trực tiếp đến tốc độ và khả năng xảy ra của một phản ứng hóa học. Những vai trò quan trọng bao gồm:
Quyết định tốc độ phản ứng hóa học:
- Các phản ứng có năng lượng hoạt hóa thấp thường xảy ra nhanh hơn vì các hạt phản ứng dễ dàng vượt qua rào cản năng lượng.
- Ngược lại, phản ứng có năng lượng hoạt hóa cao thường xảy ra chậm, cần thêm nhiệt hoặc chất xúc tác.
Ảnh hưởng đến điều kiện phản ứng:
- Hiểu rõ năng lượng hoạt hóa giúp xác định nhiệt độ, áp suất, hoặc các yếu tố cần thiết để phản ứng xảy ra hiệu quả. Điều này đặc biệt quan trọng trong các phản ứng công nghiệp, nơi hiệu suất và chi phí sản xuất là yếu tố then chốt.
Ứng dụng trong kiểm soát và tối ưu hóa:
- Năng lượng hoạt hóa là cơ sở để thiết kế các quy trình sản xuất công nghiệp. Các nhà hóa học sử dụng chất xúc tác để giảm Ea, tăng tốc độ phản ứng mà không tiêu tốn nhiều năng lượng.
3. Yếu tố ảnh hưởng đến năng lượng hoạt hóa
Năng lượng hoạt hóa không cố định mà có thể thay đổi dưới tác động của các yếu tố bên ngoài:
Nhiệt độ:
- Khi nhiệt độ tăng, các hạt phản ứng có nhiều năng lượng hơn để vượt qua rào cản năng lượng hoạt hóa, làm tăng tốc độ phản ứng.
- Ví dụ: Nấu chín thức ăn nhanh hơn ở nhiệt độ cao.

Đun nấu thức ăn ở nhiệt độ cao
Chất xúc tác:
- Chất xúc tác hoạt động bằng cách cung cấp một con đường phản ứng thay thế với năng lượng hoạt hóa thấp hơn. Điều này cho phép phản ứng xảy ra nhanh chóng mà không cần thay đổi nhiệt độ.
- Ví dụ: Trong ngành dầu khí, chất xúc tác platinum được sử dụng trong cracking dầu mỏ, giúp quá trình diễn ra hiệu quả hơn.
Bản chất của chất phản ứng:
- Các chất phản ứng có cấu trúc phân tử đơn giản thường có năng lượng hoạt hóa thấp hơn, trong khi các chất phức tạp hoặc có liên kết hóa học mạnh thường đòi hỏi năng lượng hoạt hóa cao.
4. Ứng dụng của năng lượng hoạt hóa trong thực tế
Công nghiệp hóa học: Sản xuất amoniac từ khí nitơ và hydro (quy trình Haber) yêu cầu năng lượng hoạt hóa cao. Chất xúc tác như sắt được sử dụng để giảm Ea, tăng hiệu quả sản xuất.
Công nghệ môi trường: Xử lý nước thải và khí thải: Chất xúc tác trong các phản ứng phân hủy chất ô nhiễm làm giảm năng lượng hoạt hóa, giúp xử lý chất thải nhanh hơn với chi phí thấp hơn.

Ứng dụng trong xử lý nước thải
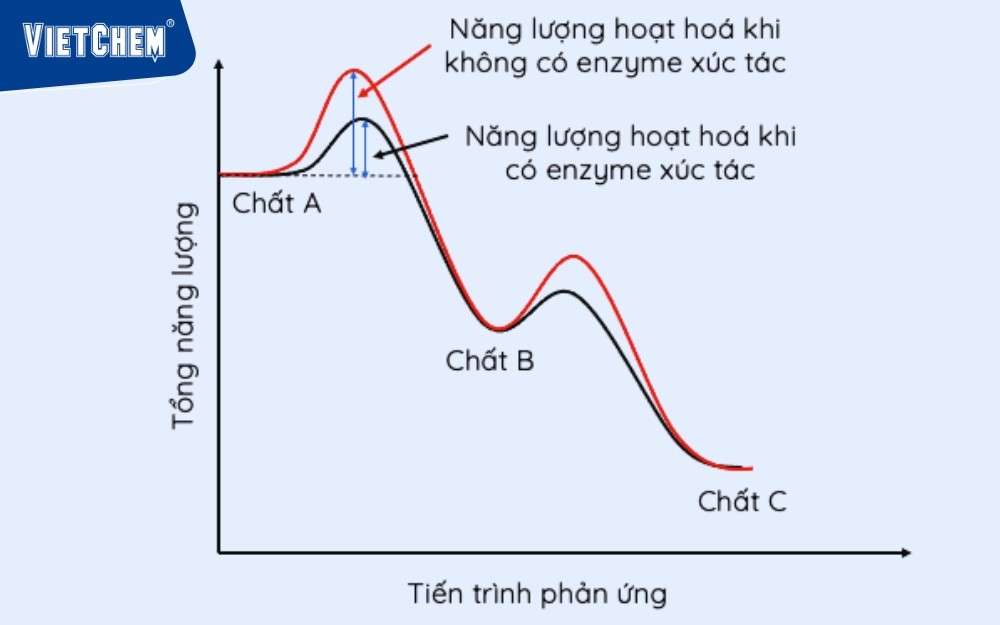
Y học và sinh học: Trong cơ thể, enzyme là chất xúc tác sinh học làm giảm năng lượng hoạt hóa của các phản ứng. Ví dụ, enzyme amylase giúp phân giải tinh bột thành glucose nhanh chóng ở nhiệt độ cơ thể.
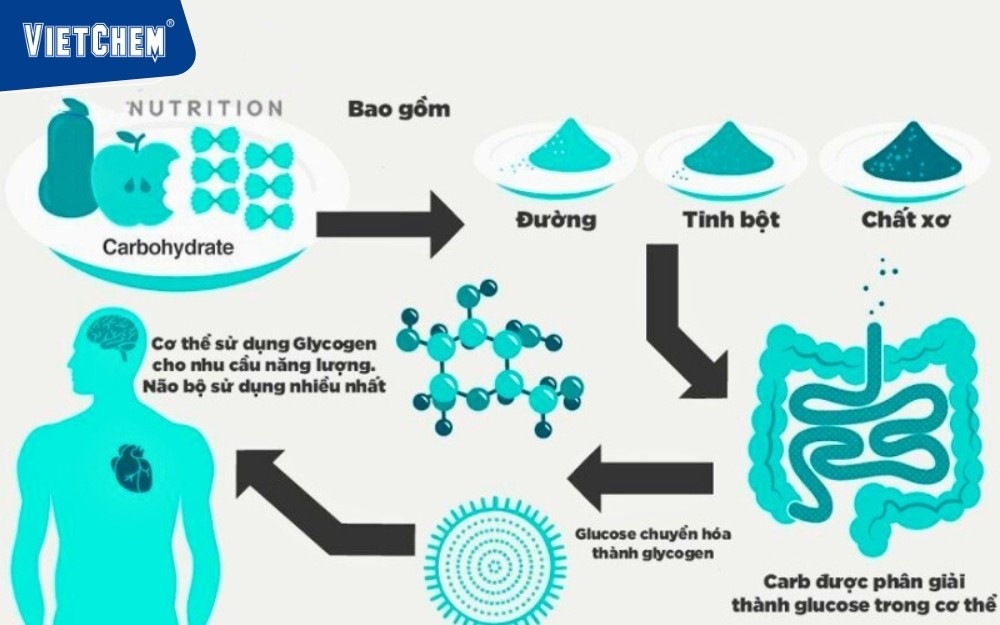
Enzyme amylase giúp phân giải tinh bột thành glucose
Năng lượng tái tạo: Trong pin nhiên liệu, giảm năng lượng hoạt hóa của phản ứng oxy hóa hydro giúp tăng hiệu suất chuyển đổi năng lượng.
Công nghệ vật liệu: Trong sản xuất vật liệu bán dẫn, việc kiểm soát năng lượng hoạt hóa cho phép điều chỉnh quá trình hình thành màng mỏng và cải thiện hiệu suất thiết bị điện tử.
5. Công thức và cách tính năng lượng hoạt hóa
Công thức tính năng lượng hoạt hóa thông qua phương trình Arrhenius:
k = A.e-Ea/RT
Ý nghĩa:
- k: Hằng số tốc độ phản ứng (tỷ lệ thuận với tốc độ phản ứng).
- A: Hệ số tần số va chạm (phụ thuộc vào bản chất của chất phản ứng).
- Ea: Năng lượng hoạt hóa (J/mol).
- R: Hằng số khí (8,314 J/mol·K).
- T: Nhiệt độ tuyệt đối (Kelvin).
Phân tích:
- Khi Ea cao, giá trị k giảm, dẫn đến tốc độ phản ứng chậm.
- Tăng nhiệt độ (T) hoặc giảm Ea (bằng chất xúc tác) sẽ làm tăng tốc độ phản ứng.
6. Tại sao năng lượng hoạt hóa quan trọng?
Tối ưu hóa quy trình công nghiệp: Hiểu năng lượng hoạt hóa giúp các nhà khoa học và kỹ sư thiết kế các điều kiện phản ứng tối ưu, giảm chi phí và tăng hiệu quả.
Tiết kiệm năng lượng: Sử dụng chất xúc tác để giảm Ea là giải pháp quan trọng trong sản xuất năng lượng sạch và phát triển công nghệ bền vững.
Phát triển công nghệ mới: Trong y học, enzyme nhân tạo được phát triển để tối ưu hóa phản ứng trong cơ thể. Trong ngành năng lượng, nghiên cứu pin nhiên liệu và vật liệu lưu trữ năng lượng tập trung vào việc kiểm soát năng lượng hoạt hóa để tăng hiệu suất.
Năng lượng hoạt hóa là yếu tố cốt lõi giúp giải thích cách các phản ứng hóa học diễn ra, đồng thời đóng vai trò quan trọng trong việc phát triển công nghệ và tối ưu hóa sản xuất. Với khả năng ứng dụng đa dạng từ công nghiệp, y học đến năng lượng tái tạo, năng lượng hoạt hóa là chìa khóa mở ra các tiến bộ khoa học và công nghệ tương lai.